Quiz Pi
C'est bien, . Vous pouvez continuer.
Beaucoup d'erreurs, vous devriez revoir les ressources.
Énoncé
Quels sont les paramètres ci-dessous qui conduisent à une augmentation de pression osmotique ?
Correction
La pression osmotique de l'eau de mer
Énoncé
Assimilons l'eau de mer à une solution de NaCl à 30 g/L. Donnez le valeur de la pression osmotique en Atm ? (vous aurez besoin de la masse molaire de NaCl mais vous avez un accés à internet !)
Correction
Explication Générale
La masse molaire de NaCl est de 58,5 g/mol. 30 g/L correspond à 0,51 mol/L. Il y a donc 0,51 mol/L de Na+ et 0,51 mol/L de Cl- car le sel est complètement dissocié. La pression osmotique est donc de ;
\(\Pi=2*0,51*10^{+3}*8,32*298=2 543 000 Pa=25,43 bar=25,1 Atm\)
On compte donc la pression osmotique des anions et des cations. 1 Atm= 1,013 bar
Vous pouvez télécharger le fichier notebook Python pour ce calcul que vous pourrez compléter pour les questions suivantes.
Fichier à télécharger
#Calcul de la pression osmotique de l eau de merc=30 # g/L
M=58.44 # g/mol
R=8.32 # J/(K.mol)
T=298 # K
L_m3=1000 # L/m3
Pa_atm=1.013e5 # Pa/Atm
C=c/M # mol/L
L_m3=1000 # L/m3
C=C*L_m3 # mol/m3
C_Na=C # mol/m3
C_Cl=C # mol/m3
Pi=(C_Na+C_Cl)*R*T # J/m3 ou Pa
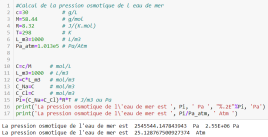
print('La pression osmotique de l\'eau de mer est ', Pi, ' Pa ', "%.2E"%Pi,' Pa')
print('La pression osmotique de l\'eau de mer est ', Pi/Pa_atm, ' Atm ')
#Calcul de la pression osmotique de l eau de mer
c=30 # g/L
M=58.44 # g/mol
R=8.32 # J/(K.mol)
T=298 # K
L_m3=1000 # L/m3
Pa_atm=1.013e5 # Pa/Atm
C=c/M # mol/L
L_m3=1000 # L/m3
C=C*L_m3 # mol/m3
C_Na=C # mol/m3
C_Cl=C # mol/m3
Pi=(C_Na+C_Cl)*R*T # J/m3 ou Pa
print('La pression osmotique de l\'eau de mer est ', Pi, ' Pa ', "%.2E"%Pi,' Pa')
print('La pression osmotique de l\'eau de mer est ', Pi/Pa_atm, ' Atm ')